2025年1月,重点实验室袁若教授课题组在《Analytical Chemistry》(IF=6.7)上在线发表了题为“Supramolecular DNA Nanodevice Assembled via RCA and HCR Cascade Reaction on Tetrahedral DNA Nanostructure for Sensitive Detection and Intracellular Imaging of Dual-miRNAs Associated with Liver Cancer.”的研究论文。

研究内容
微小RNA(miRNAs)是一类非编码小RNA分子,在调节基因表达中起着重要作用,通过与靶基因的mRNA结合来调节基因转录和翻译。miRNA的异常表达与各种癌症的发生和进展有关,影响细胞增殖、凋亡、侵袭和转移等过程。miRNA221和miRNA222是高度同源的miRNA,有报道证实它们可以共同促进癌症细胞的增殖和侵袭,它们的联合作用明显比它们的单独调节作用更显著,特别是在癌症的发生和发展中。肝细胞癌(HCC)是指起源于肝细胞的恶性肿瘤,是癌症最常见的类型,占所有癌症病例的大多数,是全球癌症死亡的第四大原因。因此,监测miRNA221和miRNA222在HCC细胞中的表达水平对于了解HCC的发展过程具有重要意义。
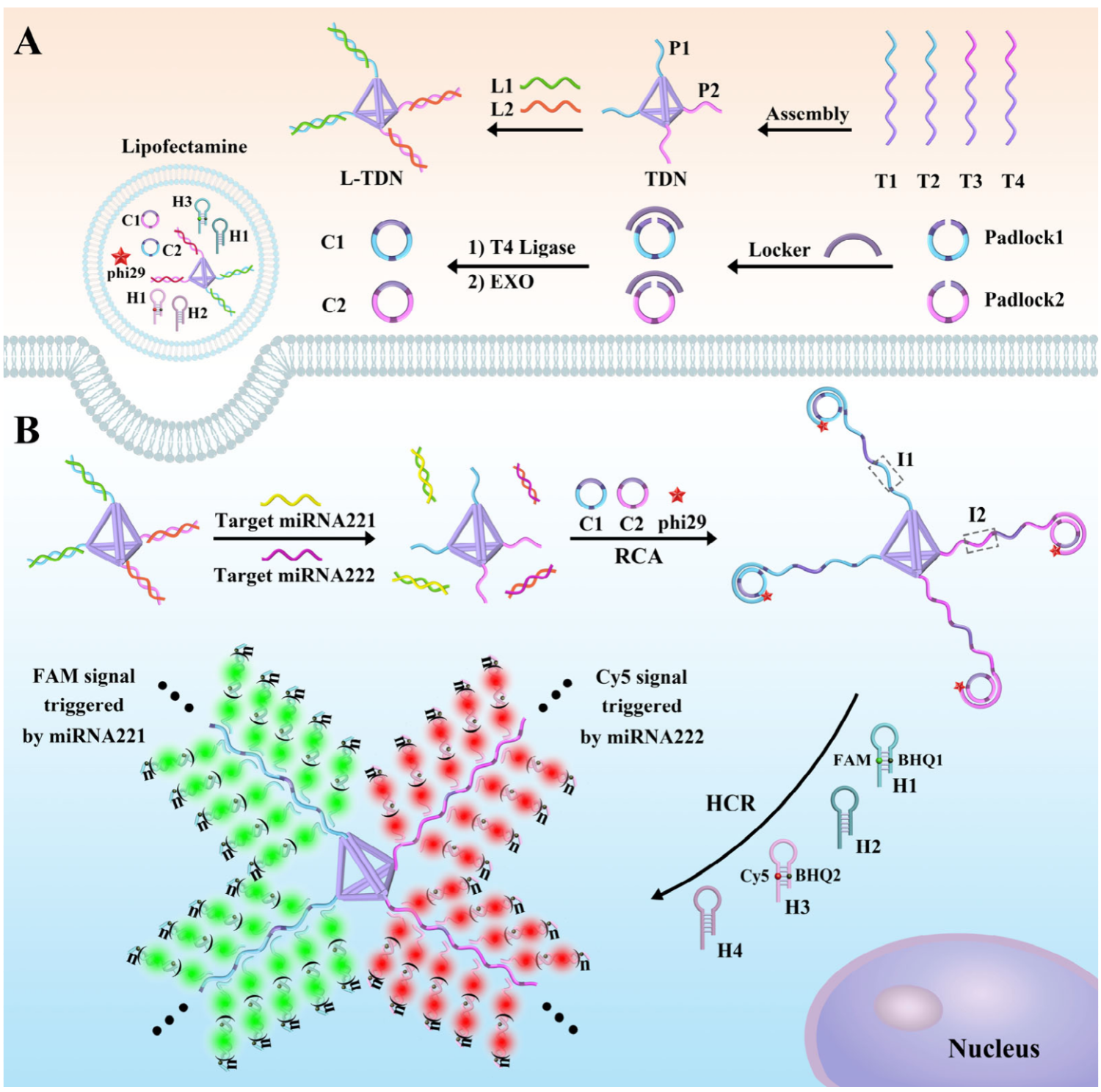
(A) Construction of the Tetrahedral DNA Nanostructure with Locked Primers (L-TDN)
(B) Illustration of Supramolecular DNA Structure Formed by the RCA and HCR Cascade Reaction on TDN for Sensitive Detection and Intracellular Imaging of Dual-miRNAs
研究意义
本研究介绍了TDN上的RCA和HCR级联反应,以形成由靶标触发的超分子DNA结构,这使得miRNA221和miRNA222能够同时进行灵敏检测和细胞内成像。与传统的TDN探针相比,超分子DNA结构实现了大量荧光探针的有序富集,解决了传统TDN结构荧光探针负载能力的局限性,显著增强了荧光信号。超分子DNA结构的形成增加了荧光探针的刚性和稳定性,减少了探针自聚集引起的自猝灭,进一步增强了荧光信号,提高了靶细胞内原位成像的准确性。基于上述特征,该纳米装置实现了正常肝细胞与具有不同转移程度的癌症肝细胞之间的区分,为细胞内肿瘤标志物的敏感和精确成像提供了一种新的工具,并具有提供更准确的癌症发展和预后信息的潜力。