近日,重点实验室许志刚/武汉大学孙志军联合在《Advanced Materials》上在线发表了题为“Innovative Biomaterials Synergize Oncolytic Virus for Elevating Tumor Immunotherapy Potency”的综述论文。系统性地探讨了如何利用创新的生物材料来解决这些难题,从而显著提升溶瘤病毒疗法的效果。这篇文章的核心观点是:将溶瘤病毒与功能各异的智能生物材料相结合,能够像给病毒穿上“特洛伊木马”一样,保护它、精准引导它,并增强其杀伤力。

研究背景
溶瘤病毒免疫治疗近年来在肿瘤治疗领域展现出巨大潜力,成为继免疫检查点抑制剂和细胞治疗之后又一备受关注的策略。溶瘤病毒能够选择性感染并裂解肿瘤细胞,同时诱导免疫原性细胞死亡,释放肿瘤抗原和危险信号,从而激活机体全身性的抗肿瘤免疫应答。然而,该疗法在临床转化中仍面临多重挑战:一方面,病毒在体内递送过程中易被血清中和抗体或吞噬细胞清除,导致肿瘤靶向效率低下;另一方面,肿瘤组织内部存在致密的细胞外基质和免疫抑制性微环境,限制了病毒的扩散与复制;此外,病毒的免疫原性可能诱发过度炎症反应,带来潜在的安全性风险。
研究内容
为突破上述瓶颈,研究人员借助生物材料科学的最新进展,为优化溶瘤病毒疗法开辟了新的技术路径。通过系统设计,各类生物材料能够与溶瘤病毒形成协同效应,显著提升肿瘤免疫治疗的效力与安全性。目前,生物材料载体主要分为非生物性与生物性两大类。
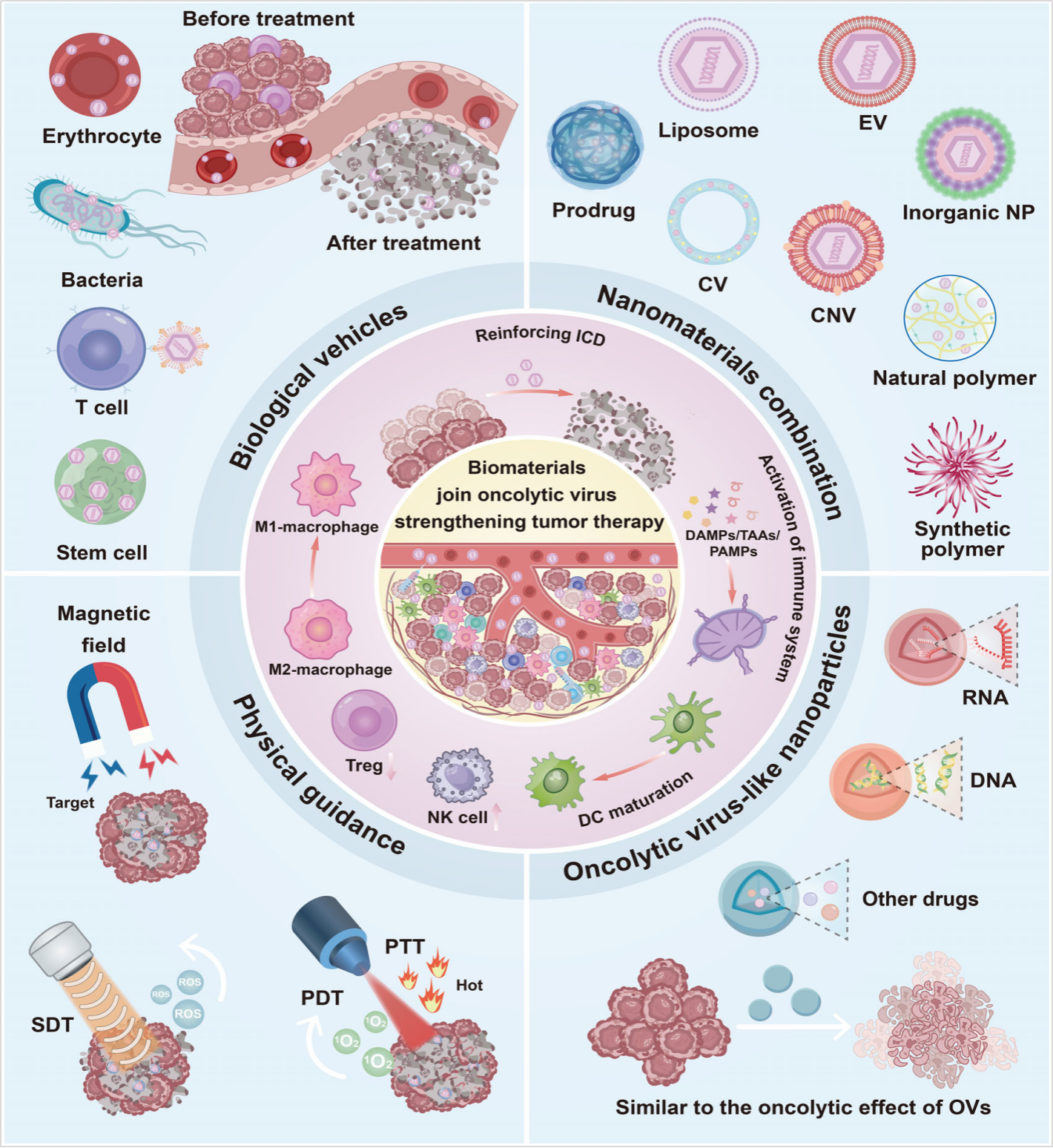
非生物性载体包括脂质体、聚合物、无机纳米颗粒、细胞外囊泡及凝聚囊泡等。其中,脂质体凭借其仿生膜结构,可高效包载病毒并实现表面靶向修饰;聚合物载体则因其分子量和结构的可设计性,能够与病毒形成稳定的静电复合物,提升递送效率;无机纳米载体(如金纳米颗粒、磷酸钙等)不仅可包载病毒,还能响应肿瘤微环境释放活性离子,诱导铁死亡或铜死亡,增强病毒复制并调控免疫应答;细胞外囊泡作为内源性载体,具备低免疫原性和天然靶向能力,可携带病毒及多种生物活性分子参与细胞间通讯。生物性载体主要包括红细胞、干细胞、血小板、中性粒细胞及肥大细胞等活细胞系统。这类载体具有优异的生物相容性、长循环时间及主动归巢能力,能够将病毒精准递送至肿瘤或转移灶,增强局部治疗效果。此外,研究人员还开发了仿病毒结构的纳米颗粒,通过模拟病毒RNA(如聚肌苷酸-聚胞苷酸)或DNA(如载药质粒)装入仿生纳米外壳中,在肿瘤部位诱导凋亡、激活STING通路或引发焦亡,产生类似溶瘤病毒的抗肿瘤免疫效应,同时避免病毒复制失控和感染风险。
前景与展望
尽管溶瘤病毒与生物材料的联合策略前景广阔,但其临床转化仍面临诸多挑战。未来,借助人工智能优化材料设计、利用高通量筛选实现个性化治疗、开发患者来源的类器官模型以加速临床转化,以及整合溶瘤病毒与免疫检查点抑制剂、CAR-T细胞疗法等多模态治疗手段,有望构建更高效、安全的肿瘤免疫治疗新范式,推动该领域向以患者为中心的精准治疗稳步迈进。