近日,重点实验室袁若/向云团队在《Journal of the American Chemical Society》上在线发表了题为“In Vivo Spatiotemporal Protection and Recognition of Circulating Tumor DNA for Early Cancer Diagnosis and Monitoring”的研究论文。提出了一种全新的“体内时空保护与识别”策略,研究者们没有在体外苦苦追寻微量ctDNA,而是直接在活体内为ctDNA派去了“贴身保镖”和“识别探针”,将可检测到的ctDNA水平提升了56.2倍,并能通过尿液实现早期肿瘤的精准监测。

研究内容
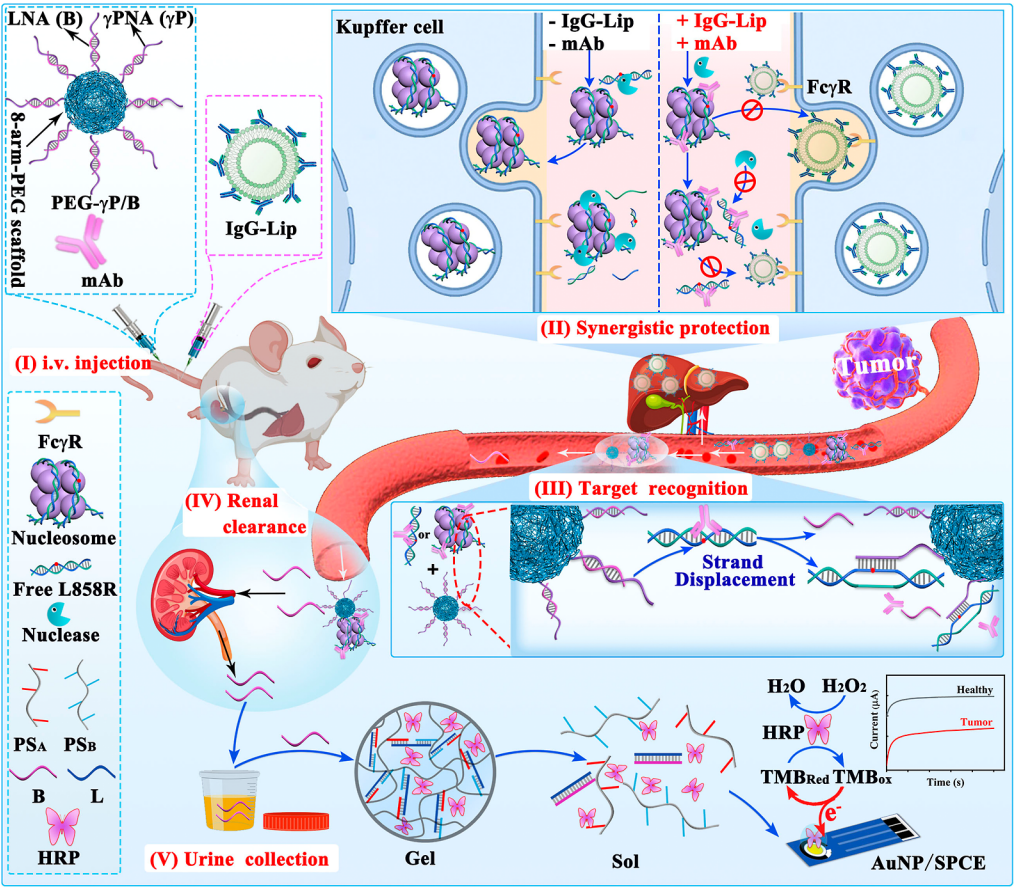
本研究提出“先饱和、后保护”的体内协同调控策略。通过注射免疫球蛋白G修饰脂质体(IgG-Lip),优先占据肝脏库普弗细胞(Kupffer cells)的Fcγ受体,暂时抑制其对ctDNA的吞噬能力,从而降低ctDNA的清除速率。在此基础上,引入抗双链DNA单克隆抗体(anti-dsDNA mAb),对循环体系中的ctDNA进行特异性结合与包裹,形成类似“保护壳”的结构,有效抵抗血液中DNase I等核酸酶的降解作用。在实现ctDNA稳定存在的基础上,构建了可在体内特异识别突变序列的核酸纳米探针体系。所设计的PEG修饰γP/B纳米探针能够在血液循环中稳定存在,并针对EGFR L858R等典型突变位点,通过立足点介导的链置换反应(toehold-mediated strand displacement reaction, TSDR)实现高特异性识别。一旦识别目标ctDNA,探针释放出尺寸较小的报告链(Probe B),实现分子层面的信号转化。进一步地,本研究将体内识别事件与体外信号检测进行巧妙耦合。释放的Probe B由于尺寸小于肾小球滤过阈值(<6 nm),可随血液循环进入肾脏并经尿液排出,实现从“血液信号”向“尿液信号”的转导。基于此,在尿液中构建DNA水凝胶放大体系,利用Probe B触发水凝胶结构解离并释放辣根过氧化物酶(HRP),通过酶催化反应产生显著增强的电化学信号,从而实现对ctDNA的高灵敏检测。
研究结果
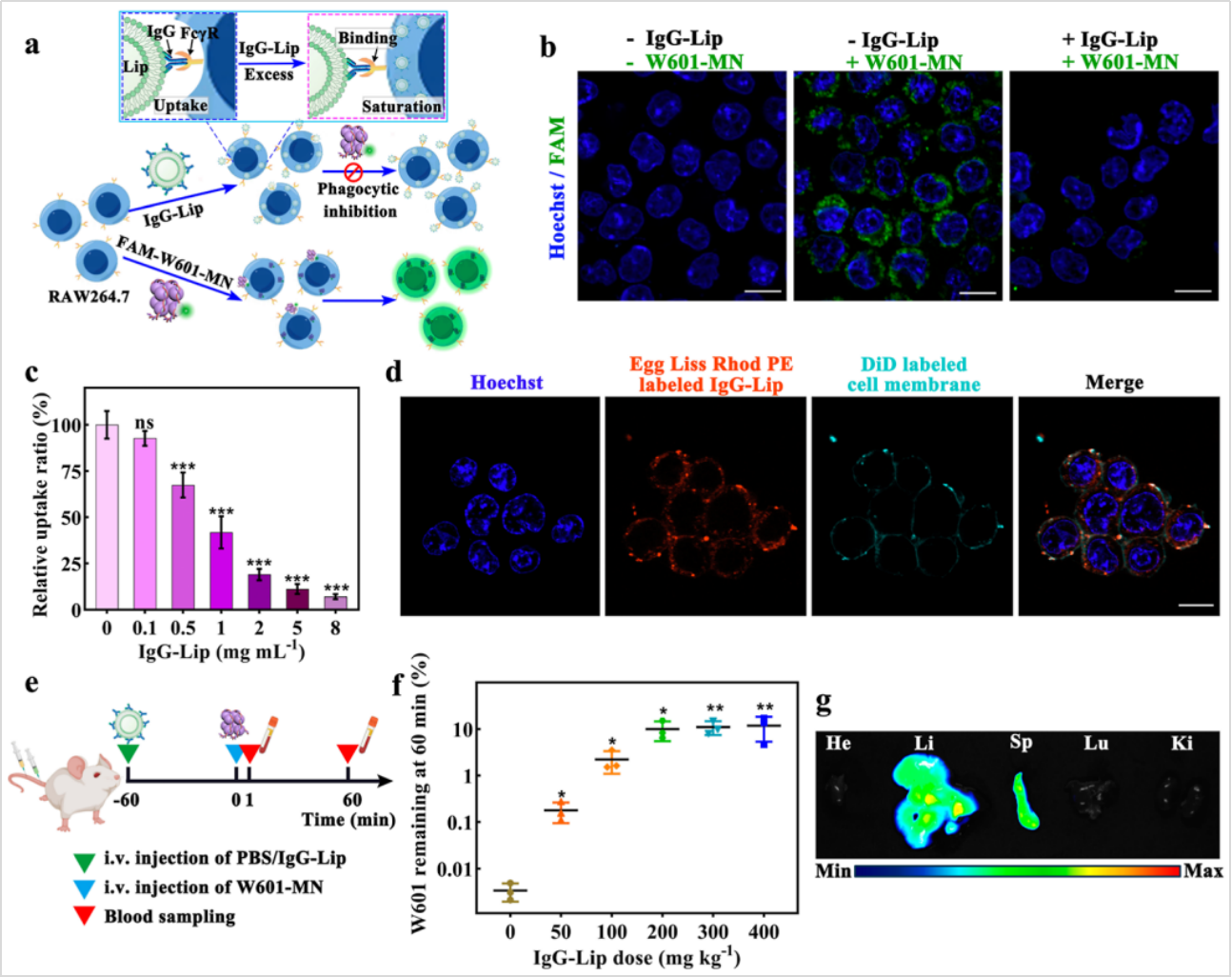
研究结果表明,所构建的体内协同保护策略显著提升了ctDNA的检测灵敏度。在肿瘤小鼠模型中,“IgG-Lip + mAb”组合使血液中可回收ctDNA水平较未处理组提高约56.2倍,有效克服了ctDNA在体内快速降解与清除的限制。基于此构建的纳米探针检测体系能够实现对EGFR突变ctDNA的高特异性识别,并成功将血液中的分子识别事件转化为尿液中的电化学信号输出。总体而言,该研究通过体内环境调控与信号放大策略的协同设计,实现了对低丰度ctDNA的高效捕获与精准检测,为无创早期癌症诊断与疗效监测提供了新的技术方案。