2024年8月,重点实验室袁若教授和周莹老师课题组在《Analytical Chemistry》(IF 6.7)上在线发表了题为“Electron-Accelerator-Induced Fast Electron Transfer for Enhancing Electrochemiluminescence of Gold Nanoclusters and Its Bioanalysis Application: A Novel Avenue for Developing High-Efficient Emitters”的研究论文。

研究背景
近年来,金属纳米簇(NCs)得益于其优异的电化学活性、良好的光稳定性和生物相容性、低生物毒性,在电致化学发光(ECL)领域引起了研究者们的广泛关注。然而,金属NCs受限于金属核和模板分子之间共价键缓慢的电荷转移造成电化学激发效率低,以及模板分子活跃的振动和转动引起的激发态能量损失,存在发光效率低的缺陷,无法满足超灵敏检测生物分子的要求。为了提高金属NCs的 ECL效率,国内外研究者主要通过聚集诱导限制模板分子的振动和转动和引入共反应促进剂提高共反应试剂与金属NCs的相互作用两种途径来实现。然而,金属NCs电化学氧化还原电子转移速率慢、传输效率低的问题尚未得到有效解决,限制了金属 NCs ECL效率的进一步提高。
研究内容
在本研究中,如下图A所示,由于发光体Au NCs和电子加速剂p型半导体CaFe2O4之间的能级匹配,在Au NCs/ CaFe2O4异质结的电化学氧化过程中,电子加速剂的价带(VB)可以提供丰富的空穴,用于将电子从Au NCs的最高占据分子轨道 (Au NCs) 快速传输到电极,产生大量的Au NCs激发态物质,以实现强的ECL。值得注意的是,与纯Au NCs相比,Au NCs/ CaFe2O4的ECL效率提高了5.4倍,电化学氧化电流提高了3.5倍。该工作解决了基于金属NCs的ECL发光体的一个关键障碍:缓慢的共价键电子传输动力学导致的较差的ECL性能,对于指导基于金属NCs的ECL发光体的合理设计和拓宽金属NCs的实际应用具有一定价值。其次,以Au NCs/ CaFe2O4作为发光体,构建了 ECL 生物测定平台用于黄曲霉毒素B1 (AFB1) 的快速痕量分析(图D),该传感器的检测限比之前的ECL生物传感器提高了3个数量级,具有良好的实际应用价值。
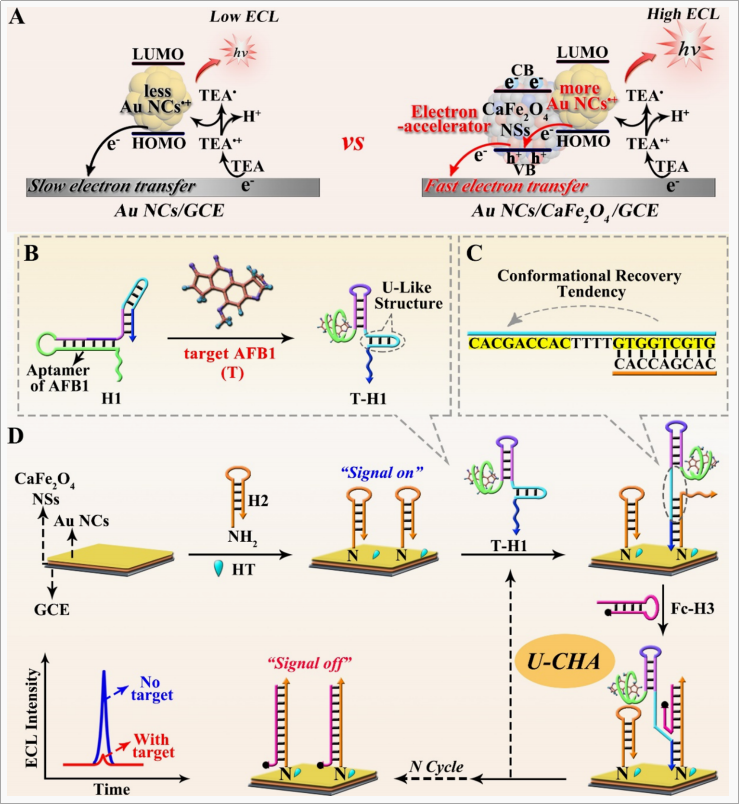
(A)ECL过程中电子转移示意图 (B)目标分子AFB1转换及
(D)ECL检测平台构建及信号响应示意图
研究意义
开发了一种新型的高效Au NCs/ CaFe2O4 ECL发光体,强调快速电子传递在ECL发射中的重要作用。为扩大金属NCs的ECL性能开辟了一条新的途径,在照明装置、超灵敏的生物传感和高分辨率ECL成像中显示出巨大的潜力。