2025年5月,重点实验室袁若教授、王海军副教授课题组在《Analytical Chemistry》(IF=6.7)上在线发表了题为“Efficient Al–H3NTB-MOG ECL Emitter with Self-Enhanced and AIECL Performance for Ultrasensitive Sensing of miRNA-141 Combined with a Y-Shaped Multiregion Dual-Drive DNA Walker”的研究论文。

研究背景
肝癌是全球范围内高发且致死率极高的恶性肿瘤之一,其早期诊断与转移过程的精准监测对改善患者预后具有重要意义。微小RNA(miRNA)作为一类非编码小分子RNA,广泛参与细胞的增殖、分化与凋亡过程,已被证实在多种肿瘤的发生、发展和转移中发挥关键调控作用。尤其是miRNA-141、miRNA-221和miRNA-222,被认为是与肝癌细胞转移和预后密切相关的重要生物标志物。高灵敏度、高特异性地检测这些miRNA,并实现其在活细胞环境中的动态成像,对于癌症的早期筛查、分型诊断以及疗效评估具有重要价值。然而,传统的核酸探针如三链DNA纳米结构(TDN)存在荧光信号弱、探针负载量有限、稳定性差等瓶颈,限制了其在细胞内精确成像和多标志物同步检测中的应用。因此,发展一种具有高负载、高稳定性、可级联信号放大的多功能DNA探针结构,成为当前肿瘤分子诊断领域的重要研究方向。
研究内容
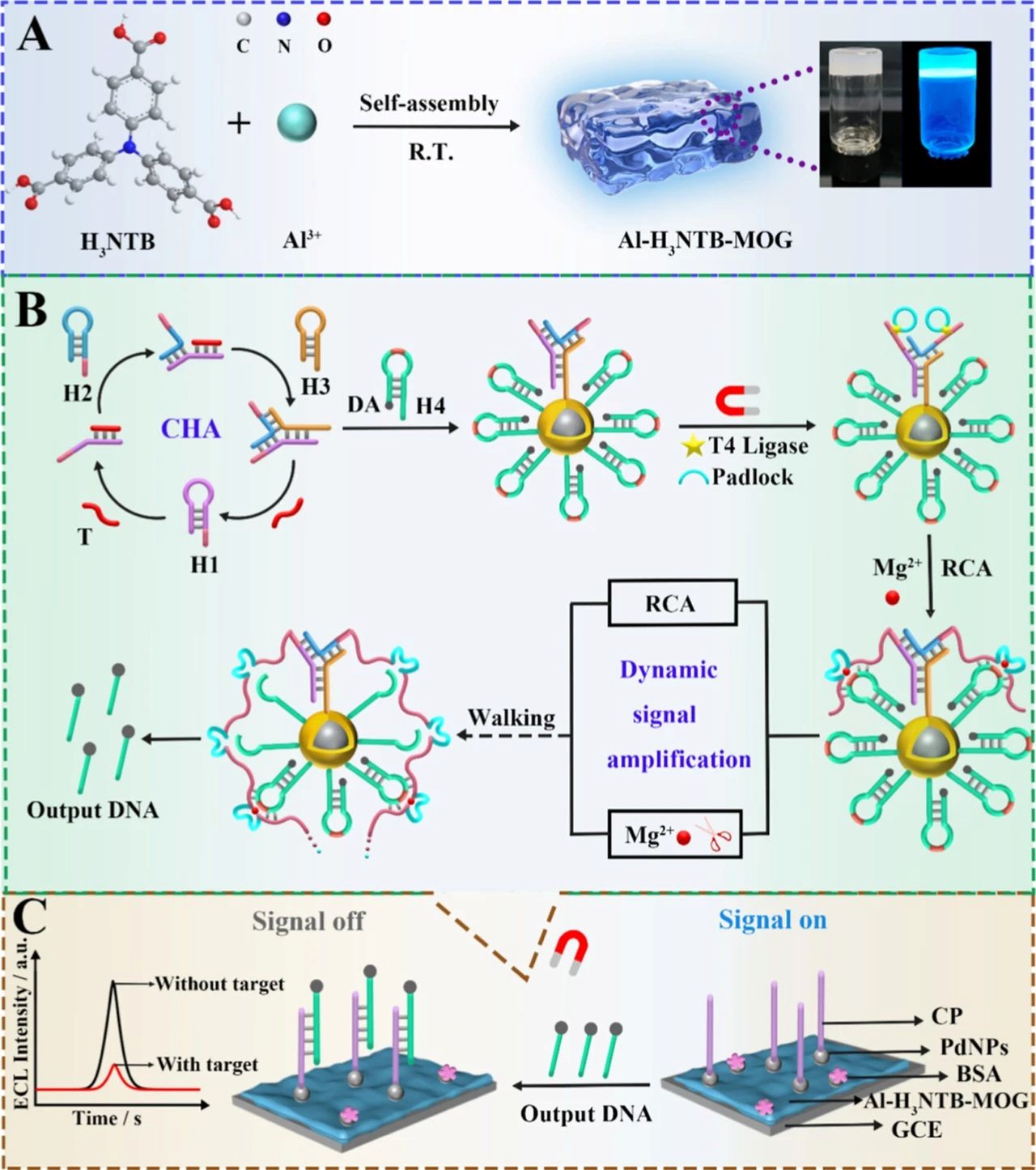
在这项工作中,使用具有自增强和聚集诱导电化学发光(AIECL)性能的 Al–H3NTB-MOG 作为高效发射体,构建了一种基于 Y 形多区域双驱动 DNA 步行者的生物传感器,用于对 miRNA-141 的灵敏检测。值得注意的是,选择 4,4′,4″-三硝基苯甲酸(H3NTB)作为具有自增强 ECL 特性的发光配体,其结构中的三胺作为共反应性三级胺。Al3+作为中心离子与 H3NTB 配位形成三维多孔凝胶结构,限制了苯分子的内部旋转和振动,并表现出优异的 AIECL 性能。更有趣的是,选择 N-2-羟乙基哌嗪-N′-乙磺酸(HEPES)作为系统缓冲液,它不仅可以稳定测试环境,还可以起到共反应补偿作用,补偿 ECL 过程中共反应基团的消耗,从而显著提高 ECL 响应的稳定性。此外,基于滚环扩增(RCA)过程和由催化发夹自组装(CHA)反应组装的 Y 形 DNA 纳米结构两端的离子裂解的协同作用,建立了一个高效的动态信号放大系统。具体来说,通过 RCA 反应形成两条具有丰富识别区域的长 DNA 链作为双驱动 DNA 步行者,它可以同时沿着预先设计的轨道行走并从两个方向剪切特定位点,有效地提高了信号放大效率。通过这种方式,构建的生物传感器实现了对 10 aM 至 1 nM 范围内的 miRNA-141 的检测,检测限低至 6.48 aM。
研究意义
本研究创新性地构建了基于TDN平台的级联反应系统,融合了滚环扩增(RCA)与杂交链反应(HCR),通过miRNA靶标的特异性识别启动超分子DNA结构的组装,从而实现对miRNA-221和miRNA-222的同时检测与成像。该超分子结构一方面提高了探针的负载能力,实现了多位点荧光信号的富集;另一方面其刚性骨架显著减少了探针间的自猝灭现象,从而增强了信号输出与成像分辨率。